HiBiT Protein Tagging System
Detect and quantify any tagged protein with a variety of sensitive methods.
The HiBiT epitope tag enables simple and flexible protein detection options. It provides a streamlined alternative for detecting epitope-tagged proteins using convenient, single-reagent-addition, bioluminescence-based methods. Compatibility with a sensitive and specific anti-HiBiT monoclonal antibody expands the utility of the HiBiT tag to include traditional antibody-based methods. All detection methods for the HiBiT tag have the dynamic range to detect proteins without overexpression, opening a world of possibilities for researchers studying protein biology.
What Is HiBiT Tagging?
HiBiT is a small, 11-amino-acid, epitope tag capable of producing a bioluminescent signal when bound to its complementation partner, LgBiT. HiBiT has unparalleled versatility and convenience with options for both simple and fast bioluminescent detection, and a sensitive and specific antibody for conventional detection methods.

Choose from Five HiBiT Detection Methods
LYTIC METHOD
Sensitive bioluminescent quantification of HiBiT-tagged proteins in cell lysates, IP complexes, or other cell-free systems.

INTRACELLULAR LIVE-CELL DETECTION
Real-time bioluminescent quantification of intracellular HiBiT-tagged proteins in live cells.
EXTRACELLULAR METHOD
Used with live cells for bioluminescent quantification of surface-expressed or secreted proteins.

ANTIBODY-BASED DETECTION
Perform traditional antibody-based detection such as western blotting, immunocytochemistry, and pull-downs of HiBiT-tagged proteins.
BLOTTING SYSTEM
Detects any tagged protein on a blot in a few minutes with a simple luminescent signal.
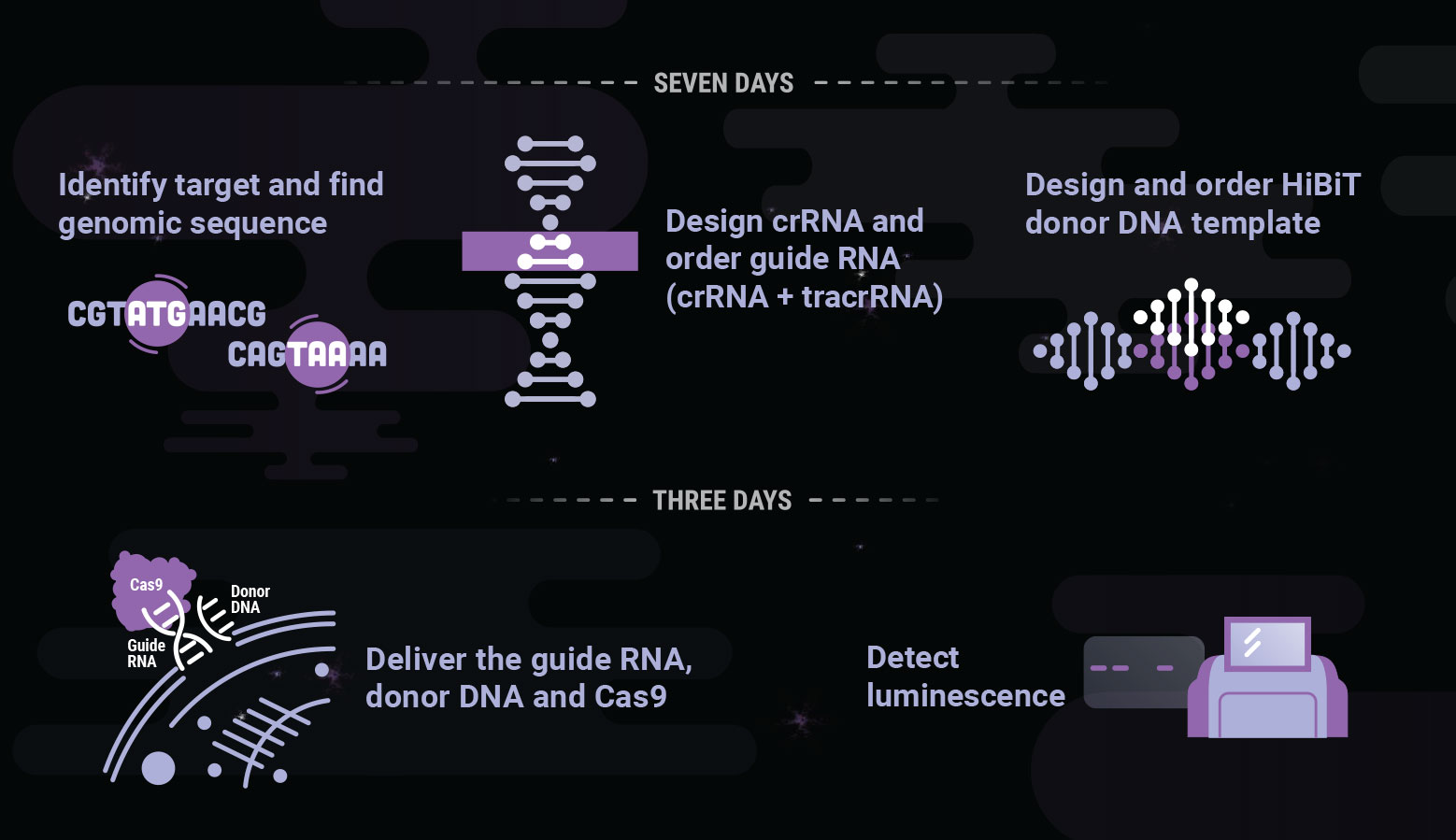
Reduce Artifacts and Study Endogenously Expressed Proteins with CRISPR Technology
CRISPR insertion allows for monitoring of proteins under endogenous expression, removing artifacts observed from overexpression and more accurately modeling the biology. The small size of HiBiT makes insertion with CRISPR efficient, and the bioluminescence method enables sensitive, quantitative detection, even of proteins with low expression. The process removes the need for molecular cloning, reducing the time it takes to insert a knock-in tag from weeks to days.
Example Applications of HiBiT Technology
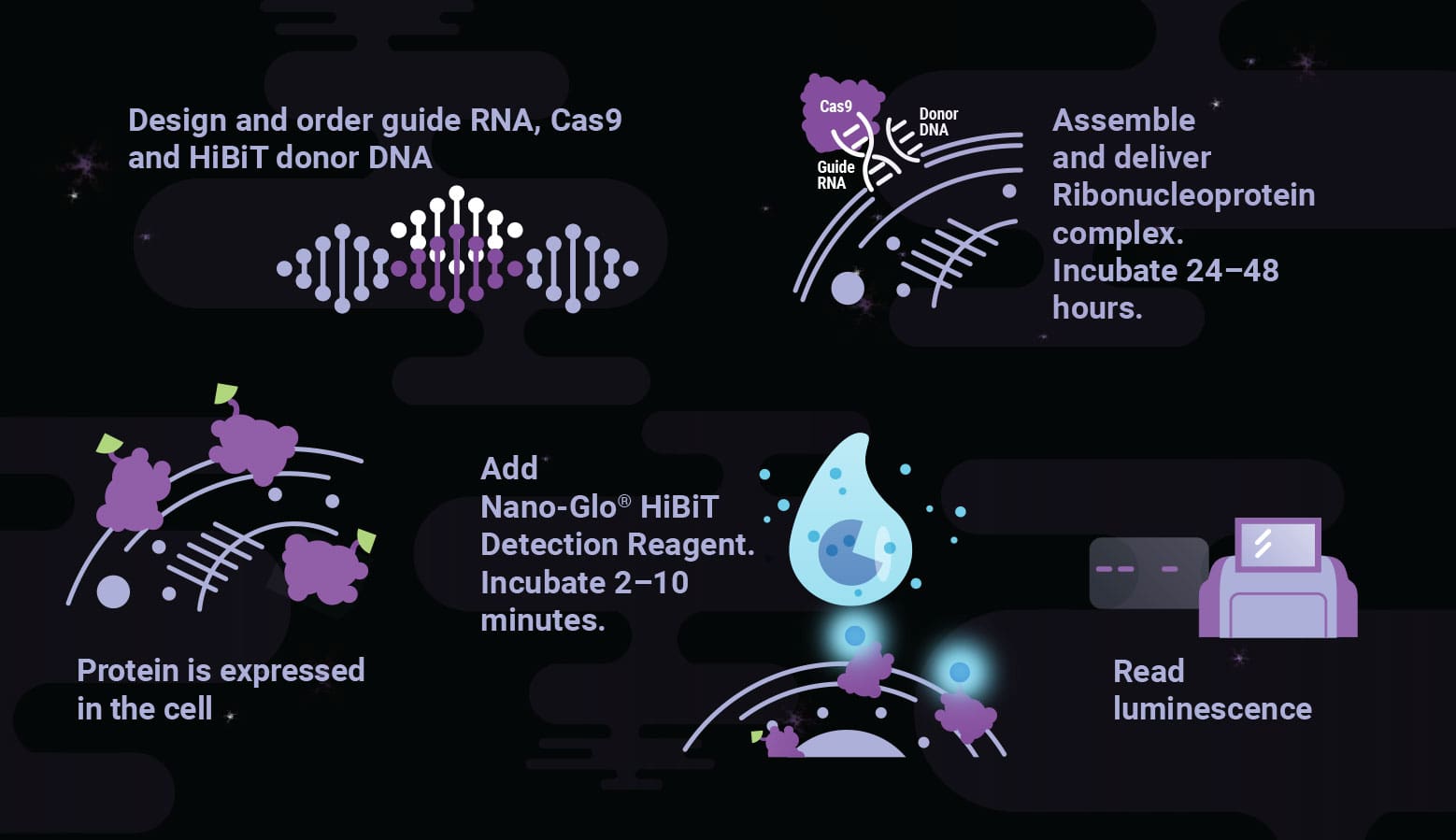
Quantify Protein Abundance and Degradation
Classic epitope tagging methods are limited in throughput or sensitivity, require high-quality antibodies and may only yield semi-quantitative results. HiBiT tagging brings the simplicity and sensitivity of bioluminescence to studies on protein abundance, quantifying proteins down to endogenous levels, even those maintained at low expression levels.
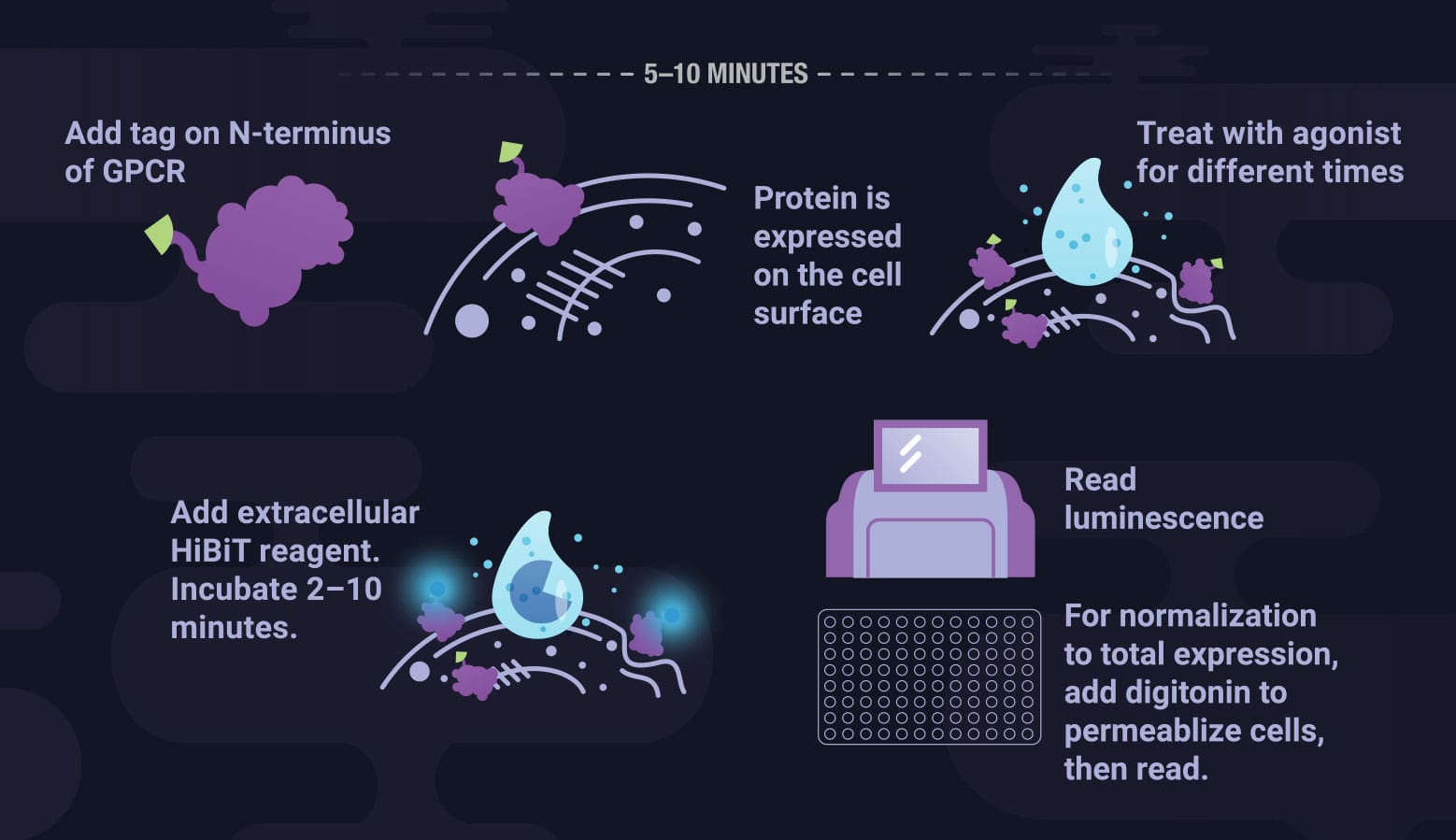
Monitor Receptor Internalization
The HiBiT detection method eliminates the need for antibody-based methods for receptor internalization studies. With HiBiT technology, the multiple antibody binding steps and associated washes are eliminated from detection protocols. Simply add the detection reagent and measure a luminescent signal.
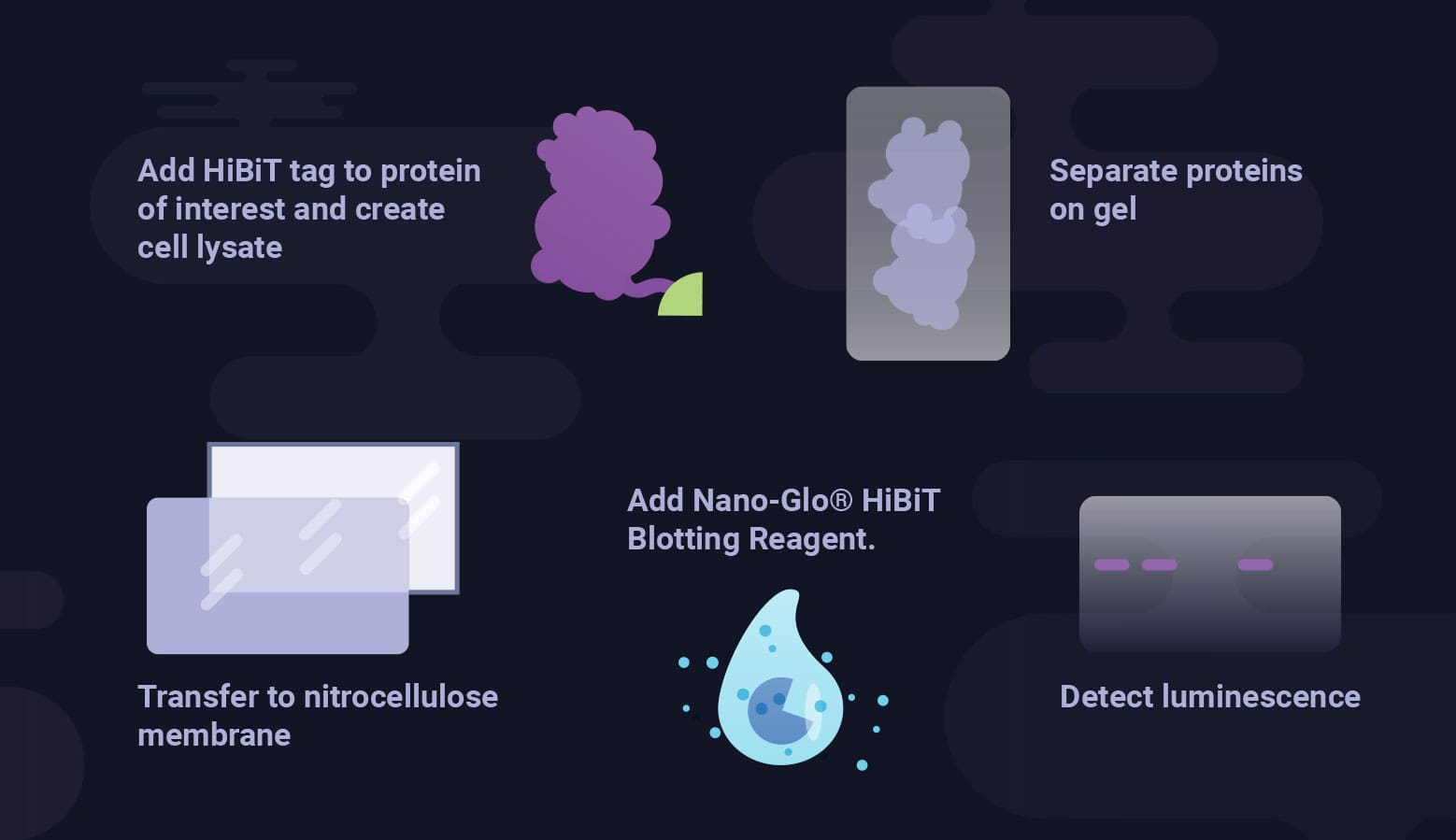
Speed and Simplify Western Blotting
The HiBiT blotting system is a sensitive and fast alternative to laborious Western blotting techniques that does not require an antibody.